Ein gemeinsames Forschungsteam der Harvard Medical School (HMS) und des MIT General Hospital gibt an, die Leistung eines Mikrodisk-Lasers mithilfe der PEC-Ätzmethode abgestimmt zu haben, was eine neue Quelle für Nanophotonik und Biomedizin „vielversprechend“ mache.
(Die Leistung des Mikrodisk-Lasers kann mittels PEC-Ätzverfahren angepasst werden.)
Auf den Gebieten vonNanophotonikund Biomedizin, MikrodiscLaserund Nanodisk-Laser haben sich als vielversprechend erwiesenLichtquellenund Sonden. In verschiedenen Anwendungen wie der photonischen Kommunikation auf Chips, der Biobildgebung auf Chips, der biochemischen Sensorik und der Quantenphotonen-Informationsverarbeitung ist eine präzise Laserleistung mit extrem schmalbandiger Genauigkeit erforderlich. Die Herstellung von Mikro- und Nanodisk-Lasern mit dieser exakten Wellenlänge in großem Maßstab stellt jedoch weiterhin eine Herausforderung dar. Aktuelle Nanofabrikationsverfahren führen zu einer zufälligen Variation des Scheibendurchmessers, was die Erzielung einer festgelegten Wellenlänge in der Massenproduktion von Lasern erschwert. Nun hat ein Forscherteam der Harvard Medical School und des Wellman Center for Lasers am Massachusetts General Hospital eine Lösung entwickelt.Optoelektronische Medizinhat eine innovative optochemische (PEC) Ätztechnik entwickelt, die es ermöglicht, die Laserwellenlänge eines Mikrodisk-Lasers mit subnanometergenauer Präzision einzustellen. Die Arbeit wurde in der Fachzeitschrift Advanced Photonics veröffentlicht.
Fotochemisches Ätzen
Berichten zufolge ermöglicht das neue Verfahren des Teams die Herstellung von Mikrodisc-Lasern und Nanodisk-Laserarrays mit präzisen, vorbestimmten Emissionswellenlängen. Der Schlüssel zu diesem Durchbruch liegt in der Anwendung der photochemischen Ätzung (PEC), die eine effiziente und skalierbare Methode zur Feinabstimmung der Wellenlänge eines Mikrodisc-Lasers bietet. In den oben genannten Ergebnissen gelang es dem Team, mit Siliziumdioxid beschichtete Indium-Gallium-Arsenid-Mikrodiscs auf einer Indiumphosphid-Säulenstruktur herzustellen. Anschließend stimmten sie die Laserwellenlänge dieser Mikrodiscs durch photochemische Ätzung in verdünnter Schwefelsäure präzise auf einen bestimmten Wert ab.
Sie untersuchten außerdem die Mechanismen und die Dynamik spezifischer photochemischer (PEC) Ätzprozesse. Schließlich übertrugen sie das wellenlängenabgestimmte Mikroscheiben-Array auf ein Polydimethylsiloxan-Substrat, um unabhängige, isolierte Laserpartikel mit unterschiedlichen Laserwellenlängen zu erzeugen. Die resultierende Mikroscheibe weist eine extrem breite Bandbreite der Laseremission auf.Laserauf der Säule kleiner als 0,6 nm und das isolierte Partikel kleiner als 1,5 nm.
Öffnung der Tür für biomedizinische Anwendungen
Dieses Ergebnis eröffnet zahlreiche neue Anwendungsmöglichkeiten in der Nanophotonik und Biomedizin. So können beispielsweise eigenständige Mikrodisk-Laser als physikalisch-optische Barcodes für heterogene biologische Proben dienen und die Markierung spezifischer Zelltypen sowie das Targeting spezifischer Moleküle in Multiplex-Analysen ermöglichen. Die zelltypspezifische Markierung erfolgt derzeit mit konventionellen Biomarkern wie organischen Fluorophoren, Quantenpunkten und fluoreszierenden Beads, die eine breite Emissionslinienbreite aufweisen. Daher können nur wenige spezifische Zelltypen gleichzeitig markiert werden. Im Gegensatz dazu ermöglicht die ultraschmale Lichtemission eines Mikrodisk-Lasers die gleichzeitige Identifizierung einer größeren Anzahl von Zelltypen.
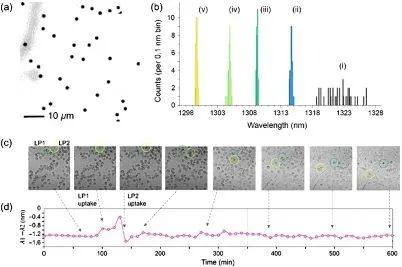
Das Team testete und demonstrierte erfolgreich präzise abgestimmte Mikrodisk-Laserpartikel als Biomarker, indem es damit kultivierte normale Brustepithelzellen (MCF10A) markierte. Dank ihrer Ultrabreitbandemission könnten diese Laser die Biosensorik revolutionieren und bewährte biomedizinische und optische Verfahren wie zytodynamische Bildgebung, Durchflusszytometrie und Multi-Omics-Analysen nutzen. Die auf PEC-Ätzung basierende Technologie stellt einen bedeutenden Fortschritt bei Mikrodisk-Lasern dar. Die Skalierbarkeit des Verfahrens sowie seine subnanometergenaue Präzision eröffnen unzählige neue Anwendungsmöglichkeiten für Laser in der Nanophotonik und in biomedizinischen Geräten sowie für Barcodes für spezifische Zellpopulationen und analytische Moleküle.
Veröffentlichungsdatum: 29. Januar 2024





